La Société internationale pour la recherche sur les cellules souches (ISSCR) a publié aujourd’hui des lignes directrices actualisées pour la recherche sur les cellules souches et son application à la médecine.
Élaborées en réponse aux récentes avancées scientifiques et cliniques, les lignes directrices révisées fournissent une série de recommandations détaillées et pratiques qui établissent des normes mondiales sur la façon dont ces technologies émergentes devraient être exploitées.
La recherche sur les cellules souches a un énorme potentiel – elle pourrait contribuer à ouvrir la voie à de nouvelles thérapies pour des affections allant de la maladie de Parkinson à l’insuffisance rénale infantile. Mais les avancées scientifiques dans ce domaine peuvent présenter des problèmes éthiques et politiques uniques, au-delà de ce qui est observé dans d’autres domaines de la recherche médicale.
La science progresse à un rythme effréné. Rien qu’au cours des deux derniers mois, nous avons vu des embryons humains modèles cultivés à partir de cellules de peau, et la création d’embryons humains-singes destinés à être utilisés dans la recherche.
L’ISSCR reconnaît depuis longtemps la nécessité de fixer des limites éthiques claires pour la recherche sur les cellules souches. Les directives précédentes ont fourni des conseils sur des techniques telles que l’utilisation d’embryons humains pour créer des cellules souches, et ont fixé les normes requises lors de l’utilisation de ces technologies pour créer de nouveaux médicaments.
Elles ont également interdit explicitement certaines pratiques, comme le clonage reproductif et la vente de thérapies non prouvées qui prétendent être faites de cellules souches.
Les lignes directrices de 2021 – une mise à jour de la version précédente, publiée en 2016 – visent à établir des normes pour les nombreuses avancées récentes dans la recherche sur les cellules souches et les embryons humains. Il s’agit notamment d’embryons chimériques contenant des cellules provenant d’humains et d’autres animaux, d’organoïdes cultivés à partir de cellules souches pour créer des tissus qui ressemblent à des organes humains particuliers, et de modèles d’embryons humains – des arrangements de cellules humaines qui imitent les premiers stades du développement de l’embryon.
Quelles sont les nouveautés?
Les lignes directrices contiennent une exigence claire selon laquelle certaines nouvelles approches de recherche sur les cellules souches ne doivent être menées qu’après un processus d’examen spécialisé. Cet examen doit être indépendant des chercheurs et inclure des membres de la communauté ainsi que des personnes ayant une expertise dans les domaines scientifiques, éthiques et juridiques pertinents.
Cela va au-delà de ce qui est généralement exigé par une université ou un institut de recherche où la recherche médicale est menée. En plus d’évaluer le mérite de la recherche proposée, les nouveaux examens devraient également examiner s’il existe d’autres moyens de faire la recherche, la source des cellules souches et la façon dont elles ont été obtenues, et le temps minimum nécessaire pour atteindre les objectifs de la recherche, en particulier en ce qui concerne les embryons humains et la recherche connexe.
Les nouvelles lignes directrices appellent à un débat sur l’opportunité de prolonger la limite actuelle de 14 jours pour l’expérimentation sur les embryons humains. Oregon Health Sciences/AP
L’examen spécialisé n’est pas un concept nouveau. Les directives précédentes l’exigeaient lorsque les chercheurs fabriquaient des cellules souches à partir d’embryons humains ou cherchaient à cultiver des embryons humains en laboratoire. Mais désormais, les chercheurs devront également demander un examen supérieur lorsqu’ils créent des embryons modèles tels que les blastoïdes, ou étudient le développement d’embryons animal-humain dans des utérus d’animaux.
Les chercheurs qui développent de nouvelles thérapies pour les maladies mitochondriales devront également demander un examen de niveau supérieur avant de tenter de transférer dans l’utérus d’une femme des embryons humains dans lesquels les mitochondries affectées (une partie de l’appareil de production d’énergie de la cellule) ont été remplacées.
Fait important, les directives révisées excluent aussi clairement certaines activités. Celles-ci continuent d’inclure le clonage reproductif et les tentatives de former une grossesse chez une femme à partir d’embryons humains génétiquement édités ou d’embryons modèles fabriqués à partir de cellules souches. Les activités interdites comprennent également l’utilisation d’ovules et de sperme fabriqués à partir de cellules souches humaines à des fins de reproduction, ou le transfert d’un embryon chimérique humain-animal dans l’utérus d’une femme ou d’un singe.
Les directives appellent également à une conversation publique sur la question de savoir si nous devrions autoriser une recherche limitée en laboratoire sur les embryons humains au-delà de la limite actuelle de 14 jours de développement. Historiquement, il n’a pas été possible de soutenir le développement embryonnaire humain hors du corps au-delà de ce stade. Cependant, les progrès récents dans la culture d’embryons humains soulèvent la possibilité que cela soit maintenant techniquement réalisable.
L’extension de la durée de culture – en termes de jours – pourrait potentiellement donner lieu à de nouveaux traitements pour les troubles du développement ou l’infertilité, mais soulèvera également des inquiétudes quant à savoir si les avantages possibles justifient cette recherche. Toute décision visant à renverser cette balise de longue date devrait être soigneusement délibérée et prendre en compte la loi existante, les valeurs de la communauté et la discussion autour de ce que devrait être la nouvelle limite.
Les lignes directrices révisées renforcent également la nécessité d’un consentement éclairé pour la collecte de matériel humain et la participation aux essais cliniques sur les cellules souches, et réitèrent qu’aucun nouveau traitement à base de cellules souches ne devrait être mis à disposition avant que sa sécurité et son efficacité ne soient testées dans le cadre d’essais cliniques bien conçus et visibles par le public. L’ISSCR continue de condamner l’utilisation commerciale de traitements à base de cellules souches non éprouvés.
Pourquoi ces lignes directrices sont-elles importantes?
Alors que la science des cellules souches est très prometteuse, il est primordial que la recherche soit scientifiquement et éthiquement rigoureuse, avec une surveillance, une transparence et une responsabilité publique appropriées.
Le fait que ces lignes directrices soient pilotées par des experts – notamment des scientifiques spécialisés dans les cellules souches, des médecins, des éthiciens, des juristes et des représentants de l’industrie – issus de 14 pays indique un profond sens des responsabilités et de l’intégrité au sein de la communauté des chercheurs, ainsi qu’une volonté de veiller à ce que la science reste en phase avec les valeurs de la communauté.
Toutefois, ces lignes directrices sont des recommandations et non des lois.
Les chercheurs devront se conformer à leurs réglementations et normes éthiques nationales ou étatiques respectives. Certains pays disposent déjà de cadres réglementaires conformes aux nouvelles recommandations. Dans d’autres endroits, il n’y a pas du tout d’orientation nationale autour de la recherche sur les cellules souches en laboratoire et en clinique, ou la loi existante touche à certaines mais pas à toutes les applications émergentes de la recherche sur les cellules souches.
Par exemple, en Australie, il existe déjà une voie établie pour l’examen de haut niveau des modèles d’embryons créés à partir de cellules souches. Cependant, cette même législation interdit actuellement toute tentative d’utiliser des techniques de transfert de mitochondries pour créer des embryons à des fins de recherche ou pour mener à bien une grossesse – deux activités autorisées par les nouvelles lignes directrices de l’ISSCR.
Plutôt que de tenter d’imposer un ensemble de règles strictes à un domaine de recherche en constante évolution, les nouvelles lignes directrices tentent d’aborder les questions émergentes et de conduire des discussions importantes au niveau national. En fin de compte, c’est le public et les régulateurs qui devront fixer les normes.
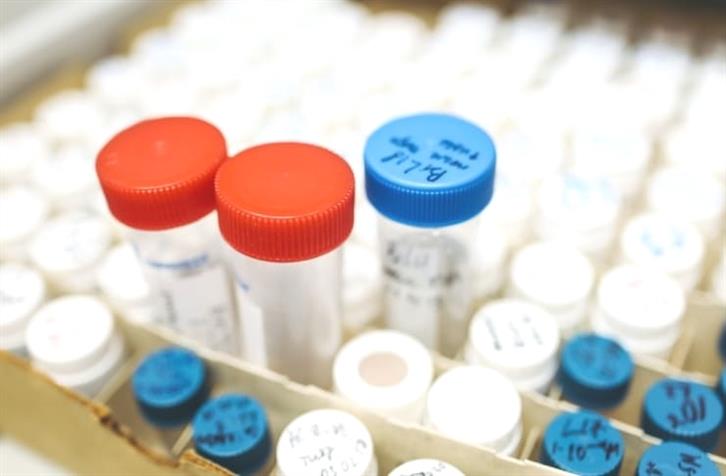
Images utilisées avec l’aimable autorisation de Pexels/Polina Tankilevitch.
Cet article est republié depuis The Conversation sous une licence Creative Commons. Lire l’article original.





Laissez une réponse
Commentaires